электродные системы для потенциометрических измерений, аналитические лабораторные и промышленные измерительные приборы
Аналитические приборы для контроля и регулирования технологических процессов, мониторинга окружающей среды
Производство лабораторных измерительных приборов было организовано в конце 1950-х годов предприятием специализирующееся на выпуске специализированных аналитических приборов. Оборудование предназначенное для контроля и регулирования технологических процессов, мониторинга окружающей среды, а также электродных систем для потенциометрических измерений.
Предприятие приборостроительной отрасли специализирующимся на выпуске лабораторных электродов и промышленных электродов.
Электроды для потенциометрических измерений
Проектирование, изготовлением различных моделей электродов для потенциометрических измерений.
При потенциометрическом (электрометрическом) методе определения активности ионов в растворе необходима электродная система, состоящая из двух электродов:
- измерительный (стеклянный) электрод, который погружается в исследуемый раствор, изменение состава которого сказывается на потенциале этого электрода,
- вспомогательный электрод (сравнения), имеющий постоянный потенциал.
Потенциал стеклянного электрода определение активности ионов водорода
Теория возникновения потенциала на примере стеклянного электрода при определении активности ионов водорода.
Стеклянный (измерительный) электрод — это система, включающая небольшой сосуд из стекла с помещенным в него внутренним буферным раствором и токоотводом. Сосуд имеет горловину из изолирующего стекла, на конце которой напаян шарик (мембрана) из специального электродного стекла, обладающего заметной электропроводностью. Токоотводом может служить внутренний хлорсеребряный электрод.
Стекло проводит электричество благодаря тому, что в нем могут мигрировать ионы щелочных металлов (натрия или лития), входящие в состав при его синтезе.
Внутренний хлорсеребряный электрод и буферный раствор - определенный потенциал
- На границе токоотвода (внутренний хлорсеребряный электрод) и внутреннего буферного раствора возникает совершенно определенный потенциал.
- Потенциал возникает и на границе стеклянной мембраны с внутренним раствором.
- В ходе измерений внутренний раствор, а значит, и сумма внутренних потенциалов остаются постоянными.
Потенциал стеклянного электрода, анализируемый раствор
Происхождение потенциала стеклянного электрода можно представить так. Когда электрод помещается в анализируемый раствор, в поверхностные слои электродного стекла из анализируемого раствора интенсивно проникают ионы водорода, вытесняя ионы содержащегося в стекле щелочного металла. Энергетическое состояние ионов в стекле и в растворе различно. Это приводит к тому, что ионы водорода так распределяются между стеклом и раствором, что поверхности этих сред (фаз) приобретают противоположные заряды, а между стеклом и анализируемым раствором возникает разность потенциалов.
Величина этой разности потенциалов зависит от рН, потому что стремление ионов водорода перейти в стекло зависит от их концентрации в растворе. Чем она больше, тем больше это стремление. Возникающая разность потенциалов так направлена, что она уменьшает стремление ионов водорода переходить в стекло. При определенной концентрации ионов водорода в растворе между стремлением их переходить в стекло и электрическим силами, которые приходится преодолевать, установится равновесие. При этом переход ионов Н+ из раствора в стекло будет осуществляться с той же скоростью, что и обратный переход из стекла в раствор.
Для измерения величины потенциала стеклянного электрода используется вспомогательный электрод (сравнения).
Потенциал вспомогательного электрода при измерении рН практически не меняется, так он зависит от концентрации ионов хлора, которая около системы Ag/AgCL (если электрод хлорсеребряный) задана и остается постоянной. Вспомогательный электрод соединен с анализируемым раствором электролитическим ключом с раствором хлористого калия. Роль этого ключа — обеспечивать проведение тока между исследуемым раствором и вспомогательным электродом, стабилизировать и свести к минимуму потенциал на этой границе.
Графически зависимость э.д.с. электродной системы, состоящей из стеклянного и вспомогательного электродов, от величины рН представляет собой прямую линию (рисунок 1).
В очень кислых растворах могут наблюдаться "кислотные ошибки", в очень щелочных — "щелочные ошибки", т.е. кривая отклоняется от линейного хода. Положение этих отклонений зависит от состава стекла и природы ионов.
На кривой зависимости э.д.с. от величины рН имеется точка (область), соответствующая такой концентрации определяемого иона, при которой потенциал электрода не зависит от температуры. Это изопотенциальная точка (рисунок 1).
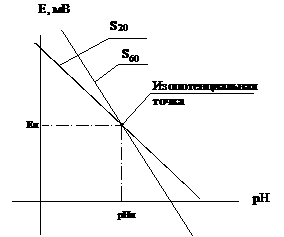
Рисунок 1. График зависимости э.д.с. электродной системы от величины рН
Уравнение этой прямой (Нернста)
Е = Е0 + S? lg a, (1)
где
Е — разность потенциалов между измерительным (стеклянным) электродом и вспомогательным электродом, мВ;
Е0 — константа, зависящая в основном от свойств электрода сравнения (стандартный потенциал электрода), мВ;
S — крутизна электродной функции электрода (Нернстовский угловой коэффициент наклона)
 (2)
(2)
где
R — газовая постоянная, Дж?моль–1? К –1;
n — заряд иона с учетом его знака;
F — Число Фарадея, Кл/моль;
N — абсолютная температура, ºК;
а — активность соответствующего иона.
Уравнение Нернста для измерения рН можно записать в виде
Е = Еи + St (рН t – рНи), (3)
где
Еи, рНи — номинальные значения координат изопотенциальной точки электродной системы, состоящей из стеклянного (измерительного) и вспомогательного электродов, соответственно, мВ, рН;
рН t — значение рН буферного раствора при температуре t , ºС;
St — крутизна водородной характеристики в мВ/рН при температуре t ºС, рассчитанная по формуле
 (4)
(4)
где
t — температура анализируемой среды, ºС;
n — заряд иона.
Крутизна электродной системы St зависит от температуры; при температуре 25ºС и десятикратном изменении активности определяемого иона она равна 59,16 мВ для однозарядных ионов и 29,56 для двухзарядных ионов. Однако обычно крутизна электродной функции меньше теоретического значения, что обусловлено присутствием мешающих примесей или старением жидкостного электрода.
Для удобства оценки реальной крутизны электродной системы St реал, как правило, используют безразмерный коэффициент К S , учитывающий отклонение реальной величины крутизны от теоретического значения;
 (5)
(5)
где
St реал — реальное значение крутизны электродной функции, мВ/рН;
St — теоретическое значение крутизны электродной функции, рассчитанное по формуле (4), мВ/рН.
Коэффициент К S, в основном равный 0,8…1,2, позволяет учитывать отклонение крутизны электродной системы St реал от теоретического значения.
pH электроды не запаянной конструкции
Производство и выпуск простейших электродов не запаянной конструкции (рисунок 2) только для измерения величины рН в узком диапазоне.

Рисунок 2. Электрод не запаянной конструкции
В лабораторных стеклянных электродах не запаянной конструкции, особенно при перепадах температур анализируемой среды, может нарушаться герметичность, внутренний буферный раствор взаимодействует не только со стеклом корпуса электрода, но и и другими материалами, которые обеспечивают герметичность (резина, смола и др.). В результате этого внутренний раствор меняет свой состав, что ведет к быстрому изменению контрольного потенциала электрода и изменению координат изопотенциальной точки.
В настоящее время мы выпускаем более сложные стеклянные электроды запаянной конструкции не только для измерения величины рН в широком диапазоне от -0,5 до 14 рН, но и для измерения других ионов.
pH электроды запаянной конструкции
Выпуск электродов запаянной конструкции.

Рисунок 3. Электрод запаянной конструкции
Преимущества электродов запаянной конструкции (рисунок 3). Внутренний буферный раствор, заполняющий корпус электрода, находится в запаянной стеклянной колбе, он не соприкасается ни с какими другими материалами, кроме стекла, и поэтому сохраняет свой состав даже при резких перепадах температур анализируемой среды, в результате чего потенциал электрода длительное время остается практически без изменений, что положительно сказывается на работоспособности электродов.
электроды измерительные (стеклянные, мембранные, редоксметрические) и вспомогательные (сравнения).
Проектирование и выпуск электродов для потенциометрических измерений как измерительные (стеклянные, мембранные, редоксметрические), так и вспомогательные (сравнения).
Для измерения величины рН предлагаем использовать модели электродов по области назначения в лабораторных условиях, в промышленных условиях, специальные электроды:
в лабораторных условиях:
- электроды запаянной конструкции ЭСЛ-43-07, ЭСЛ-43-07СР, ЭСЛ-45-11 для температур от 0 до 40 ºС;
- электроды запаянной конструкции ЭСЛ-63-07, ЭСЛ-63-07СР, ЭСЛ-15-11 для температур от 25 до 100 ºС;
- комбинированные стеклянные лабораторные электроды ЭСКЛ-08М.1 , ЭСКЛ-08М для температур от 0 до 50 ºС, изменение диффузионного потенциала на электролитическом ключе вспомогательного электрода при переносе электрода из кислоты в щелочь не превышает ±1 В;
в промышленных условиях:
- электроды запаянной конструкции ЭСП-04-14 для температур от 0 до 40 ºС;
- электроды запаянной конструкции ЭСП-01-14 для температур от 25 до 100 ºС;
- электрод запаянной конструкции ЭСП-31-06 для температур от 70 до 150 ºС;
- электрод запаянной конструкции ЭС-71-11 — стерилизуемый, диапазон измерения величины рН от -0,5 до 12 рН при 25 ºС (электрод без стерилизации можно использовать для температур от 15 до 80 ºС). Электродное стекло, используемое для изготовления электрода ЭС-71-11, позволяет производить измерения в растворах с величиной рН до -0,5 рН (в растворах, содержащих серную кислоту);
специальные электроды:
- электрод 5М2.840.019 запаянной конструкции — для анализаторов АН-72529/60,
- электрод 5М2.840.074 запаянной конструкции — для анализаторов АС-7932.
Осуществляется продажа ионоселективных стеклянных электродов:
- электроды стеклянные ЭСЛ-51-07, ЭСЛ-51-07СР запаянной конструкции — для измерения активной концентрации ионов натрия Na+ и ионов серебра Ag+,
- электрод стеклянный ЭС-10-07 запаянной конструкции — для измерения активной концентрации ионов натрия Na+, в комплекте с приборами типа рNа-205 измеряет активную концентрацию ионов натрия в химически обессоленной воде и конденсате пара котлов высокого давления ;
- электрод сульфидсеребряный ЭСС-01 — для определения концентрации сульфид-иона S–2 в промышленных условиях, в том числе в сульфатных щелоках целлюлозно-бумажного производства, а также для измерения активной концентрации ионов серебра Ag+,
- и ионоселективные мембранные электроды:
- электрод аргентитовый ЭА-2 — для измерения активности сульфидных ионов (величины р S) и может быть применен в промышленных датчиках при автоматическом контроле концентрации сульфидных ионов р S в водных растворах; применяется в выпускаемых нами сигнализаторах СЦ-2,
- электроды мембранные ЭМ- I-01, ЭМ- I-01СР — для измерения активной концентрации ионов I –,
- электроды мембранные ЭМ- CN-01, ЭМ- CN-01СР — для измерения активной концентрации ионов CN– ; могут применяться в химической и золотодобывающей промышленности, при анализе и очистки сточных вод гальванических цехов, на обогатительных фабриках, в процессах флотации с применением цианистых солей; применяется в выпускаемых нами сигнализаторах СХ-2,
- электроды мембранные ЭМ- Cl-01, ЭМ- Cl-01СР — для измерения активной концентрации ионов Cl; могут применяться в химической промышленности при контроле технологических процессов, при анализе и очистке сточных вод гальванических цехов, в научных исследованиях, медицине,
- электроды мембранные ЭМ- NO3-07, ЭМ- NO3-07СР — для измерения активной концентрации ионов NO–3; могут применяться для анализа почв, продукции растениеводства, пищевой промышленности; могут быть использованы в лабораторной практике в различных отраслях промышленности, биологии, медицины, охраны окружающей среды,
Для измерения окислительно-восстановительных потенциалов выпускаем электроды, как с использованием драгоценных металлов, так и со специальным электродным стеклом: ЭПВ-1, ЭПВ-1СР, ЭТП-02, ЭПЛ-02, ЭО-01 .
- Электроды ЭПВ-1, ЭПВ-1СР, ЭПЛ-02 являются наиболее распространенными электродами. В обратимых окислительно-восстановительных системах позволяют проводить определение концентраций компонентов до 10–5н. В сравнении с электродом ЭТП-02 имеют меньшую чувствительность к примесям и большой срок службы, в особенности при повышенных температурах и в средах, содержащих твердые частицы. Однако газообразные кислород и водород, каталитические яды оказывают влияние на потенциал электрода. Электроды имеют ограничения по шкале окислительных потенциалов, прежде всего в области сред с низкими окислительными потенциалами из-за обратимой системы Н2 / Н+ на платине.
- Электрод ЭТП-02 обладает высокой чувствительностью и малой поляризуемостью за счет того, что индикаторная часть выполнена из мелкодисперсной платины. Это позволяет в ряде случаев проводить измерения в малобуферных растворах систем. Высокая чувствительность электрода из-за активности мелкодисперсной платины к газообразным водороду и кислороду, а также к ядам (соединениям серы, мышьяка, ртути) ограничивает его использование в разбавленных растворах и растворах, содержащих газообразные водород и кислород, каталитические яды.
- Электрод ЭО-01 (с электронно-проводящим электродным стеклом) в большинстве растворов обратимых редокс систем имеет меньшие токи обмена, чем платиновая проволока. Как и с электродами ЭПВ-1, с электродом ЭО-01 можно проводить определение концентраций в обратимых системах вплоть до концентраций 10–5н, но время установления равновесных потенциалов несколько больше. Для электрода ЭО?01 не характерны каталитические эффекты, не проявляется влияние газообразных кислорода и водорода. Электрод позволяет производить измерения в растворах со слабо выраженными окислительно-восстановительными свойствами (в растворах с относительно низкой буферной емкостью). Из-за сравнительно невысокой химической устойчивости электродного стекла ограничена область применения электрода ЭО-01 по величине рН (от 3 до 11 рН при прямых потенциометрических измерениях).
Преимущества стеклянных электродов
Измерительные стеклянные электроды с внутренним заполнением — запаянной конструкции , о преимуществах электродов запаянной конструкции говорилось ранее.
Кроме того, для исключения влияния статического электричества на показания измерительных высокоомных лабораторных электродов: ЭСЛ-43-07, ЭСЛ-43-07СР,
ЭСЛ-63-07, ЭСЛ-63-07СР, ЭСЛ-45-11, ЭСЛ-15-11, ЭСЛ-51-07, ЭСЛ-51-07СР, ЭС-10-07, а также ЭСП-31-06, ЭС-71-11 мы используем не только бесшумный экранированный коаксиальный кабель с сопротивлением изоляции более 1012 Ом, но и экранируем внутреннюю часть электрода металлическим экраном, что уменьшает дрейф потенциала.
В эксплуатационных документах мы указываем линейный диапазон ионной характеристики электродов не только для температур 25 ºС (20 ºС), но и для максимальных температур анализируемой среды (требование государственных стандартов) , что позволяет потребителю правильно выбрать необходимый для своих условий электрод, в то время как другие изготовители нормируют линейный диапазон ионной характеристики только для температуры 25 ºС.
В нормативных и эксплуатационных документах на измерительные электроды мы указываем оптимальные диапазоны по температуре анализируемой среды и пределам измерений, что позволяет потребителю правильно выбрать электрод для обеспечения длительной эксплуатации электродов без ухудшения их характеристик.
Для всех стеклянных рН — электродов мешающими ионами являются ионы щелочных металлов — в основном ион натрия, поэтому мы нормируем верхние значения линейного диапазона водородной характеристики рН-электродов при мешающем влиянии ионов натрия, равном 0,1 моль/л (требование государственных стандартов) .
В отсутствии мешающих ионов большинство стеклянных рН электродов имеют линейную функцию вплоть до рН = 14.
Кроме измерительных электродов предлагаются вспомогательные электроды (сравнения) как для промышленных условий, так и для лабораторных.
Это лабораторные электроды ЭВЛ-1М3.1, ЭВЛ-1М4 , электроды промышленные ЭВП-08, ЭХСВ-1 , электроды 5М2.840.072 5М2.840.072 для лабораторных анализаторов АН?7529/60 и АС-7932.
Электрод сравнения 2-го разряда ЭСО-01
Осущетствляется выпуск единственного на постсоветском пространстве образцового электрода сравнения 2-го разряда ЭСО-01.
Вспомогательные электроды (сравнения): ЭВЛ-1М3.1, ЭВЛ-1М4, ЭВП-08,
ЭХСВ-1, ЭСО-01, выпускаемые заводом, являются насыщенными хлорсеребряными, поэтому потенциал электродов стабильный, не зависит от изменения концентрации внутреннего раствора при изменении температуры, температурный коэффициент потенциала электродов не меняет свой знак в зависимости от температуры раствора.
Потенциалообразующая часть лабораторных электродов расположена в верхней части корпуса электродов и не погружается в контролируемый раствор, поэтому влияние температуры контролируемого раствора минимально.
Через электролитический ключ вспомогательного электрода осуществляется связь вспомогательного электрода с анализируемым раствором. На электролитическом ключе возникает диффузионный потенциал. Диффузионный потенциал вспомогательного электрода различается в зависимости от конструкции электролитического ключа и скорости истечения электролита через электролитический ключ. При низкой или неравномерной скорости истечения электролита через ключ меняется диффузионный потенциал, что приводит к неправильным измерением. При проведении точных измерений надо заботиться о постоянстве диффузионных потенциалов.
Практика утверждает, что при использовании ключей с небольшой скоростью истечения диффузионный потенциал нестабилен. Причиной нестабильности диффузионного потенциала керамических ключей моет быть также закупорка пор солевого мостика грязью, осадками или кристаллами хлористого калия. Изменение диффузионного потенциала на керамическом ключе может достигать 12 мВ.
Электролитический ключ: изменение диффузионного потенциала при переносе из кислоты в щелочь не превышает ± 1 мВ
В лабораторных вспомогательных электродах ЭВЛ-М3.1, ЭВЛ-1М4, а также комбинированных лабораторных электродах ЭСКЛ-08М, ЭСКЛ-08М.1 электролитический ключ выполнен таким образом, что изменении диффузионного потенциала на ключе при переносе электрода из кислоты в щелочь (и наоборот) не превышает ± 1 мВ , что важно при проведении точных анализов.
Использование электродов с керамическими ключами при проведении анализов с использованием магнитной мешалки и потенциометрическом титровании также проблематично, так как наблюдается дрейф потенциала и невозможно определить конечную точку титрования.
При использовании электродов: вспомогательных ЭВЛ-1М3.1, ЭВЛ-1М4 и комбинированных электродов ЭСКЛ-08М, ЭСКЛ-08М.1 указанные дефекты не наблюдаются.
Если вытекающий из вспомогательных лабораторных электродов раствор КС l является мешающим (например, для измерения ионов Cl– ), то предприятие выпускает:
- специальный электролитический ключ 1Е5.184.412 для электрода ЭВЛ-1М3.1;
- электролитическую ячейку 1Е5.184.307 для электрода ЭВЛ-1М4.
Конструкция ключа (ячейки) практически исключает попадание в исследуемые растворы хлористого калия, вытекающего из вспомогательных электродов. Эти ключи (ячейки) очень просто отмыть от заливаемого в них раствора и можно использовать для многих вспомогательных электродов.
При таких измерениях в соответствии с рисунком 4 измерительный электрод (1) помещается в стакан (3) с анализируемым раствором (2) непосредственно, а вспомогательный электрод (4) — через электролитический ключ (ячейку) (5). Тип раствора, заливаемого при этом в электролитический ключ (ячейку) (5), определяется указаниями в паспортах на применяемые измерительные ионоселективные электроды или исследователем.

Рисунок 4. Проведение измерений в растворах, если вытекающий раствор КCl является мешающим
- Измерительный электрод;
- Анализируемый раствор;
- Стакан;
- Вспомогательный электрод ЭВЛ-1М3.1 или ЭВЛ-1М4;
- Электролитический ключ 1Е5.184.412 для электрода ЭВЛ-1М3.1 или электролитическая ячейка 1Е5.184.307 для электрода ЭВЛ-1М4.
При проведении измерений необходимо соблюдать следующие условия:
- уровень раствора в электролитическом ключе (5) должен быть выше уровня анализируемого раствора (2) в стакане (3),
- уровень раствора KCl в электроде (4) должен быть выше уровня раствора в электролитическом ключе (5).
Серийно выпускаемые электроды можно использовать и для проведения измерений в пробах малого объема .
Для этого мы выпускаем специальные ячейки для микроизмерений (рисунок 5), которые входят в комплект поставки приборов таких приборов, как И-160.

Рисунок 5. Проведение измерений в пробах малого объема (микроизмерения)
- Вспомогательный электрод ЭВЛ-1М3.1 или ЭВЛ-1М4;
- Специальная крышка;
- Стакан;
- Измерительный электрод;
- Микродоза — анализируемый раствор;
- Электролитический ключ 5М5.129.001.
Они представляют собой стакан (3) с крышкой (2), в которой имеются отверстия для установки вспомогательного электрода (1), термометра или термокомпенсатора и электролитического ключа (6).
Электролитический ключ для микроизмерений (6) имеет форму цилиндра со сферическим дном, в нижней части которого имеется небольшое удлинение с впаянной нитью, обеспечивающей электрическую связь электролитического ключа со вспомогательным электродом.
В соответствии с рисунком 5 микродоза (анализируемый раствор) и рабочая часть измерительного электрода помещаются в полую часть ключа (6), а вспомогательный электрод погружается в стакан (3), заполненный насыщенным раствором KCl. Уровень раствора KCl в стакане (3) должен быть таким, чтобы обеспечивать надежный контакт с нитью электролитического ключа (6), а уровень анализируемого раствора в ключе (6) — выше уровня раствора КСl в стакане.
- Электроды соответствуют основополагающим стандартам по электродной продукции:
- Все электроды внесены в реестры средств измерений республики Беларусь и Российской Федерации, многие электроды внесены в реестры средств измерений Украины и Казахстана.
- Осущетслена большая работа по созданию и внедрению на предприятии системы высокоэффективных методов управления производством и получен Сертификат соответствия международным стандартам серии ИСО 9000.
Наличие собственных уникальных производств изготовления электродов, основанных на современных технологиях, процесс подготовки производства, выбора материалов, строжайшее соблюдение техпроцессов, отработанных в течение десятилетий, пооперационный контроль каждой операции при изготовлении электродов, тщательный подбор кадров позволяет изготавливать продукцию высокого качества.
Отлаженное производство как измерительных, так и вспомогательных электродов для потенциометрических измерений с технологией, отработанной и усовершенствованной в течение десятилетий
Практически все производители электродной продукции на территории Российской Федерации регулярно закупают различные модели электродов.
Купить рН-метры, pH meters в Санкт-Петербурге
pH метры Россия
Подробнее... Купить pH метры производства Россия - pH meter made in Russia в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить портативные, стационарные pH метры Россия в Санкт-Петербурге по выгодной цене. компактные модели рН-метров, приборов для измерения водородного показателя.карманные рН-метры
Подробнее... Купить карманные рН-метры - pocket pH meters в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Легкие и удобные устройства предназначены для оперативного определения кислотности или щелочности среды / определения уровня pH среды в полевых условиях, когда использование более громоздких лабораторных «портативных рН-метров»; «стационарных рН-метров» приборов зат...рН-метры для пищевой промышленности
Подробнее... Приборы для анализа пищевых продуктов - купить рН-метры для пищевой промышленности - pH meters for food industry в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Универсальные измерительные приборы контроля качества продуктов питания применяются в различных лабораториях и производстве. Купить прибор в Санкт-Петербурге по выгодной цене. рН-метры. В каталоге ХИМСНАБ-СПБ представлены...Купить электроды для измерения pH, анализаторы pH-электроды для рН-метров
Выносные электроды предназначеных для проведения измерений в лабораторных и полевых измерений рН, определения окислительно-восстановительного потенциала, удельной электрической проводимости и температуры воды, водных растворов. Анализаторы состоят из измерительного преобразователя и комбинированных датчиков (первичных преобразователей), обеспечивающих измерение параметров водной среды. Измерительные приборы отличает высокая производительность и точность осуществляемых измерений.
Купить электроды и датчики, electrodes and sensors в Санкт-Петербурге
Ион-селективные электроды
Подробнее... Купить Ион-селективные электроды - Ion-selective electrodes в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить Ион-селективный электрод в Санкт-Петербурге по выгодной цене. Проведение лабораторных ионометрических исследований, ионометрический анализ образцов требует наличия анализаторов и специализированного лабораторного оборудования: ионоселективного электрода, вспомогательного...pH-электроды, электроды для измерения pH
Подробнее... Купить pH-электроды (pH-electrodes) лабораторные измерительные устройства, анализаторы жидкости, растворов, воды и водных сред используемые для получения точных и воспроизводимых показаний приборов, опредлеление кислотности или щелочности выраженной в виде pH. В комании ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93 можно приобрести рН-электроды для рН-метров, анализаторов воды предназначе...датчики ОВП, редокс-электроды
Подробнее... Индикаторные элементы для проведения измерения окислительно-восстановительных потенциалов. В обратимых окислительно-восстановительных системах позволяют проводить определение концентрации компонентов. Специализированные электроды и датчики ОВП, редокс-электроды имеют особые электрохимические характеристики для потенциометрических измерений, регистрации ОВП растворов. Измерительное оборудован...датчики проводимости
Подробнее... Купить многодиапазонные датчики проводимости - conductivity sensors для кондуктометров использующих выносной (сменный) электрод в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить датчик проводимости в Санкт-Петербурге по выгодной цене. Специализированные электроды и датчики, electrodes and sensors с подключаемым кабелем используемые для определения проводимости и солесодержания в вод...кислородные датчики
Подробнее... Купить кислородные датчики - oxygen sensors для стационарных и портативных оксиметров в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Модели стандартных полярографических датчиков растворенного кислорода применяемых в настольных и портативных приборах. Отдельные модели датчиков кислорода состоят из платинового катода, серебряного анода и фторопластовой мембраны. Конструкции датчика делаю...электроды вспомогательные (сравнения)
Подробнее... Купить электроды вспомогательные (сравнения) - auxiliary electrode (comparison) в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Лабораторный вспомогательный или опорный электрод, заполненный концентрированным раствором КСl - электролит является вторым по значимости элементом измерительного прибора «рН-метра» . Данный тип электрода позволяет создать опорную точку, относитель...Предствленная информация на страницах данного интернет-сайта и в каталоге продукции носит исключительно информационный характер и ни при каких условиях не является публичной офертой, определяемой положениями Статьи 437 (2) Гражданского кодекса РФ. Для получения подробной информации о наличии и стоимости указанных товаров и (или) услуг,обращайтесь к менеджерам отдела продаж: форма обратной связи, e-mail, телефон.
Реализация продукции для сельского хозяйства, химической, строительной, нефтегазовой, металлургической, текстильной, кожевенной, и других отраслей промышленности.
Рады проконсультировать Вас по подбору рН-метров, рН-электродов и другого оборудования.

Менеджер ХИМСНАБ-СПБ
Предлагаем широкие возможности для комплектации химической продукцией производства и исследовательских лабораторий в различных отраслях промышленности.
«ХИМСНАБ-СПБ» - Ваш надежный поставщик
Поставка химической продукции и лабораторного оборудования является ключевым направлением деятельности компании с 1996 года.
Компания «ХИМСНАБ-СПБ» успешно осуществляет поставку широкого спектра лабороторного оборудования, приборов и другой химической продукции на рынке Северо-Запада Российской Федерации.
О компании Химснаб-СПБ




