Степень диссоциации слабых электролитов меньше единицы, диссоциация протекает обратимо
Степень диссоциации слабых электролитов меньше единицы (с < со). Их диссоциация протекает обратимо:
- СН3СООН ↔ СНзСОО − + Н + ;Н 2 СО 3 ↔ Н + + НСОз−
Константу равновесия электролитической диссоциации слабого электролита называют константой диссоциация. Например, при 298 К
- с -с +
-
К дСН3СООН =
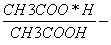 =1,8*10 -5
=1,8*10 -5 - c+ c-
-
К дН2СО3 =
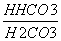 = 4,4.10 -7
= 4,4.10 -7
Сравнивая значения К д СН3СООН и К д Н2СО3" , можно сказать, что у угольной кислоты способность к диссоциации на ионы меньше, чем у уксусной.
Степень (а) и константа диссоциации (K д ) слабого электролита связаны зависимостью (закон Оствальда):
-
К д = а 2 со =_а 2 ____=
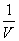 ,
, - (1-a) (1-a)V"
- где V = 1/с о - разведение раствора, л/моль.
В растворах электролитов осуществляются межионные взаимодействия, обусловленные силами притяжения и отталкивания. Наиболее заметны межионные взаимодействия в растворах сильных электролитов.
Для количественной характеристики межишных взаимодействий используется ионная сила раствора I (полусумма произведений концентраций всех ионов, присутствующих в растворе, на квадрат их заряда):
- I= 1/2∑с i zi2
Зная ионную силу раствора I, можно найти коэффициент γ, позволяющий определить некоторую величину а (активность), формально заменяющую концентрацию с:
- ai = γ i с i и γ, - коэффициент активности иона, который является функцией ионной силы раствора I и заряда иона zi .
Количественной характеристикой способности растворов электролитов проводить электрический ток является электрическая проводимость. Различают удельную 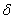 и молярную μ электрическую проводимость.
и молярную μ электрическую проводимость.
Удельная электрическая проводимость раствора 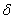 (См • м -1 ) -величина, обратная удельному электрическому сопротивлению:
(См • м -1 ) -величина, обратная удельному электрическому сопротивлению:
-
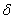 = 1/р (1)
= 1/р (1)
Молярная электрическая проводимость раствора μ (См 2 *моль -1 ) - это электрическая проводимость такого объема раствора, в котором содержится один моль растворенного вещества:
-
μ =_
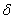 1000
1000 - с о (2)
μ возрастает с уменьшением с 0 (или с увеличением V), достигая некоторого предельного значения.
Проводниками электрического тока в растворах электролитов являются ионы, поэтому электрическая проводимость тем выше, чем больше ионов в растворе. Известно, что концентрация ионов в растворах слабых электролитов тем больше, чем больше степень диссоциации электролита а. Установлено, что между электрической проводимостью и степенью диссоциации существует взаимосвязь, вторая выражается формулой
-
а= μ/ μ
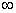
-
где μ
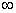 - табличная величина (табулируются значения μ
- табличная величина (табулируются значения μ 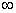 „ при 291 или 298 К).
„ при 291 или 298 К).
Итак, чтобы вычислить степень диссоциации электролита (а) в растворе заданной концентрации при данной температуре, необходимо знать молярную электрическую проводимость (μ) этого раствора при той же температуре. Молярную электрическую проводимостъ рассчитывают по уравнению (2). Удельная электрическая проводимость раствора электролита, являясь величиной, обратной удельному сопротивлению раствора (р), может быть вычислена по экспериментально найденному значению электрического сопротивления (R) раствора электролита заданной концентрации при данной температуре.
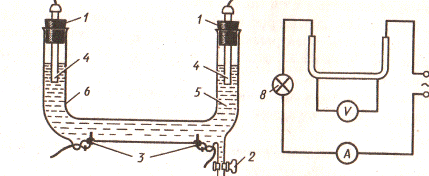
Рис. 1. Ячейка для измерения электрического сопротивления раствора (а) и схема ее включения (б):
- пробки; 2 - кран для слива жидкости; 3 - платиновые электроды; 4-угольные электроды; 5 - исследуемый раствор; 6 - сосуд; 7 - источник | переменного тока; 8 - лампочка
Для измерения сопротивления раствора электролита при Т = const служит ячейка, изображенная на рис.1, а*. Через элекролит пропускают переменный электрический ток; схема включения ячейки в сеть приведена на рис. 1, б.
Сосуд 6 изготовляется из стеклянной трубки диаметром 12-15 мм и длиной 25-30 см. Концы трубки загнуты вверх. В горизонтальный участок трубки на расстоянии 10-12 см друг от друга впаивают два небольших кусочка платиновой проволоки (диам., 0,1 мм, длина 5-6 мм). К платиновым проволочкам припаивают тонкие медные проволочки, которые для большей прочности укрепляют на стеклянных выступах в нижней части сосуда. К ним припаивают провода, соединенные с вольтметром.
Платиновые электроды 3 служат для измерения падения напряжения в растворе электролита 5 в сосуде 6.
Ток подводится к раствору при помощи угольных электродов 4, закрепленных в резиновых пробках 1. Пробки вынимают при заполнении сосуда раствором; для сливания растворов служит кран 2. Через раствор пропускают переменный ток / (220 В). Для уменьшения тока в цепь последовательно с сосудом 6 включают дополнительное сопротивление - электрическую лампочку 8. Ток через раствор пропускают только во время измерений, чтобы не было разогревания раствора, изменяющего величину его электрического сопротивления.
Для измерения тока в цепи и падения напряжения между электродами 3 используют тестер (авометр), являющийся одновременно амперметром и вольтметром и позволяющий измерять как ток, так и напряжение в широком диапазоне их значений. Напряжение измеряется при параллельном включении вольтметра, а ток - при последовательном включении амперметра (рис. 1, б).
Измерив ток в цепи (7) и падение напряжения между электродами (U), можно вычислить сопротивление столба жидкости, заключенной между электродами:
- R = U/I, (4)
- и удельное сопротивление раствора электролита р:
- р = Rs/l, (5)
- где s - поперечное сечение проводника; l - его длина.
Отношение s/l называют "постоянной прибора". Эксперимент начинают с определения постоянной прибора. Для этого используют раствор электролита с известным удельным сопротивлением р (чаще всего 0,1 М раствор КС1, удельное сопротивление которого при 291 К и при 298 К равно соответственно 89,4 и 77,6 Ом*см). Измерив значения U и I в цепи, вычисляют R по уравнению (4), а затем постоянную прибора по уравнению (5).
Далее заменяют раствор хлорида калия исследуемым раствором и снова измеряют U и I. Зная постоянную прибора и сопротивление исследуемого раствора R, рассчитывают удельное сопротивление раствора электролита р и удельную электрическую проводимость а по уравнению (1).
Пользуясь соотношением (2), вычисляют μ исследуемого раствора.
Зная предельную молярную электрическую проводимость водного раствора исследуемого электролита μ 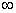 , рассчитывают по уравнению (3) степень диссоциации а.
, рассчитывают по уравнению (3) степень диссоциации а.
Купить рН-метры, pH meters в Санкт-Петербурге
pH метры Россия
Подробнее... Купить pH метры производства Россия - pH meter made in Russia в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить портативные, стационарные pH метры Россия в Санкт-Петербурге по выгодной цене. компактные модели рН-метров, приборов для измерения водородного показателя.карманные рН-метры
Подробнее... Купить карманные рН-метры - pocket pH meters в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Легкие и удобные устройства предназначены для оперативного определения кислотности или щелочности среды / определения уровня pH среды в полевых условиях, когда использование более громоздких лабораторных «портативных рН-метров»; «стационарных рН-метров» приборов зат...рН-метры для пищевой промышленности
Подробнее... Приборы для анализа пищевых продуктов - купить рН-метры для пищевой промышленности - pH meters for food industry в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Универсальные измерительные приборы контроля качества продуктов питания применяются в различных лабораториях и производстве. Купить прибор в Санкт-Петербурге по выгодной цене. рН-метры. В каталоге ХИМСНАБ-СПБ представлены...Купить электроды для измерения pH, анализаторы pH-электроды для рН-метров
Выносные электроды предназначеных для проведения измерений в лабораторных и полевых измерений рН, определения окислительно-восстановительного потенциала, удельной электрической проводимости и температуры воды, водных растворов. Анализаторы состоят из измерительного преобразователя и комбинированных датчиков (первичных преобразователей), обеспечивающих измерение параметров водной среды. Измерительные приборы отличает высокая производительность и точность осуществляемых измерений.
Купить электроды и датчики, electrodes and sensors в Санкт-Петербурге
Ион-селективные электроды
Подробнее... Купить Ион-селективные электроды - Ion-selective electrodes в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить Ион-селективный электрод в Санкт-Петербурге по выгодной цене. Проведение лабораторных ионометрических исследований, ионометрический анализ образцов требует наличия анализаторов и специализированного лабораторного оборудования: ионоселективного электрода, вспомогательного...pH-электроды, электроды для измерения pH
Подробнее... Купить pH-электроды (pH-electrodes) лабораторные измерительные устройства, анализаторы жидкости, растворов, воды и водных сред используемые для получения точных и воспроизводимых показаний приборов, опредлеление кислотности или щелочности выраженной в виде pH. В комании ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93 можно приобрести рН-электроды для рН-метров, анализаторов воды предназначе...датчики ОВП, редокс-электроды
Подробнее... Индикаторные элементы для проведения измерения окислительно-восстановительных потенциалов. В обратимых окислительно-восстановительных системах позволяют проводить определение концентрации компонентов. Специализированные электроды и датчики ОВП, редокс-электроды имеют особые электрохимические характеристики для потенциометрических измерений, регистрации ОВП растворов. Измерительное оборудован...датчики проводимости
Подробнее... Купить многодиапазонные датчики проводимости - conductivity sensors для кондуктометров использующих выносной (сменный) электрод в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Купить датчик проводимости в Санкт-Петербурге по выгодной цене. Специализированные электроды и датчики, electrodes and sensors с подключаемым кабелем используемые для определения проводимости и солесодержания в вод...кислородные датчики
Подробнее... Купить кислородные датчики - oxygen sensors для стационарных и портативных оксиметров в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Модели стандартных полярографических датчиков растворенного кислорода применяемых в настольных и портативных приборах. Отдельные модели датчиков кислорода состоят из платинового катода, серебряного анода и фторопластовой мембраны. Конструкции датчика делаю...электроды вспомогательные (сравнения)
Подробнее... Купить электроды вспомогательные (сравнения) - auxiliary electrode (comparison) в ХИМСНАБ-СПБ, контактный телефон +7-812-337-18-93. Лабораторный вспомогательный или опорный электрод, заполненный концентрированным раствором КСl - электролит является вторым по значимости элементом измерительного прибора «рН-метра» . Данный тип электрода позволяет создать опорную точку, относитель...Предствленная информация на страницах данного интернет-сайта и в каталоге продукции носит исключительно информационный характер и ни при каких условиях не является публичной офертой, определяемой положениями Статьи 437 (2) Гражданского кодекса РФ. Для получения подробной информации о наличии и стоимости указанных товаров и (или) услуг,обращайтесь к менеджерам отдела продаж: форма обратной связи, e-mail, телефон.
Реализация продукции для сельского хозяйства, химической, строительной, нефтегазовой, металлургической, текстильной, кожевенной, и других отраслей промышленности.
Рады проконсультировать Вас по подбору рН-метров, рН-электродов и другого оборудования.

Менеджер ХИМСНАБ-СПБ
Предлагаем широкие возможности для комплектации химической продукцией производства и исследовательских лабораторий в различных отраслях промышленности.
«ХИМСНАБ-СПБ» - Ваш надежный поставщик
Поставка химической продукции и лабораторного оборудования является ключевым направлением деятельности компании с 1996 года.
Компания «ХИМСНАБ-СПБ» успешно осуществляет поставку широкого спектра лабороторного оборудования, приборов и другой химической продукции на рынке Северо-Запада Российской Федерации.
О компании Химснаб-СПБ